Introdução à Termodinâmica
Introdução
Termodinâmica é o estudo de como o calor consegue realizar trabalho (isto é, transferir energia) e por consequência ser utilizado para os mais variados propósitos, como mover máquinas. Ao longo do tempo, diferentes estudos e as famosas leis da termodinâmica foram desenvolvidas.
Esse exemplo foi uma das grandes razões pelo desenvolvimento acelerado da termodinâmica na ciência nos últimos séculos, começando pela Revolução Industrial, que foi impulsionada por máquinas à vapor.
.*](./images/introduction_thermodynamics/introduction_thermodynamics_steam_engine_2.gif)
Um motor à vapor, provavelmente o exemplo clássico da termodinâmica. A pressão exercida pelo vapor exerce uma força que move os pistões. GIF sob CC-BY, via Wikimedia Commons.
Para darmos inicio ao estudo da termodinâmica, iremos primeiro discorrer sobre gases, o gás ideal e as transformações gasosas, o meio mais comum e prático de trabalho termodinâmico que temos à disposição.
Gases
Chamamos gases os corpos físicos formados por partículas em movimento, com grande quantidade de energia cinética que, ao contrário dos vapores, não conseguem ser condensados com facilidade a partir de mudanças em sua temperatura e pressão.
No estudo dos gases, a teoria cinética dos gases nos fornece o conceito de gás ideal, um gás hipotético cujas partículas estão sempre em um movimento aleatório e constante. A velocidade dessas partículas está relacionada com a temperatura desse gás.
Embora nenhum gás real possua essas características, o gás ideal se torna uma aproximação cada vez melhor da realidade a medida que aumentamos a temperatura e diminuímos a pressão sobre o gás analisado.
Geralmente em nossos estudos, utilizamos como aproximação o gás ideal, pela facilidade que isso nos oferece, embora em pesquisas mais sérias, essa aproximação se torna tão eficaz e novos métodos devem ser adotados.
Se você pudesse ver um gás bem de perto, veria várias partículas “voando” livremente em colisões perfeitamente elásticas. Essa visão é explicada pela “Teoria Cinética dos Gases”. Domínio público, via Wikimedia Commons.
A formulação dessa teoria cinética dos gases iniciou-se nos princípios da termodinâmica, que surgiu da mecânica estatística e suas formulações a partir do modelo de gás mencionado anteriormente permitu grandes avanços na compreensão física de seus comportamentos.
A Lei dos Gases Ideais
A chamada Lei dos Gases Ideais foi enunciada no começo do século XIX pelo físico francês Émile Clapeyron, a partir da combinação das leis empíricas de Boyle, Charles, Avogadro e Gay-Lussac e, posteriormente, derivada por dois alemães, August Krönig e Rudolf Clausius, que utilizaram-se da mecânica estatística.
A relação, conhecida por ser uma equação de estado, — pois relaciona as variáveis do gás num instante específico — é enunciada geralmente nas formas abaixo, com $k_B$ se referindo à constante de Boltzmann $(k_B \approx 1.38 \cdot 10^{-23} \text{ J/K})$, $N_A$ ao número de Avogadro $(N_A \approx 6.02 \cdot 10^{23})$ e $R$ a chamada constante do gás ideal $(R = k_B \cdot N_A \approx 8.314 \text{ J / mol K})$. Além das constantes, temos como variáveis a pressão, o volume e a temperatura do gás.
Essas variações existem em consideração dos diferentes objetivos que uma medição ou um cálculo pode ter, com a constante do gás ideal mais utilizada em escala macroscópica e a constante de Boltzmann empregada em análises na escala de partículas, como será exemplificado na próxima seção.
Um efeito dessa mudança de constante empregada surtido nos cálculos é o cuidado devido com a consistência das unidades.
Pressão, velocidade e energia
Conceitualmente, a grandeza pressão é definida como a razão entre a magnitude de uma força e a área que esta afeta. No caso dos fluidos (gases e líquidos), ela pode ser compreendida como uma medida da “força” que suas partículas aplicam ao colidirem com seu recipiente.
À partir da TCG, a relação acima pode ser derivada para gases monoatômicos, com $m$ sendo a massa do gás, $v_m$ a velocidade média das partículas do gás e $V$ seu volume.
.*](./images/introduction_thermodynamics/introduction_thermodynamics_pressuredcooker.jpeg)
As panelas de pressão se utilizam dessa propriedade, e seu efeito nos pontos de ebulição, para economizar gás durante o cozimento. Imagem sob CC-BY-SA, via Wikimedia Commons.
Diferentes maneiras existem para calcular a velocidade das partículas de um gás — cada uma com uma nuance diferente.
De início, temos a velocidade mais provável $(v_p)$ de ser possuída por qualquer molécula, calculada a partir da expressão abaixo, considerando $R$ a constante geral dos gases, $T$ a temperatura em Kelvin e $M$ a massa molar da substância.
Uma outra grandeza, a velocidade média $(v_m)$ é definida como o valor esperado (”média”) da distribuição estatística de velocidades. Em uma das formas de calcular, temos $m$ como a massa de uma partícula do gás.
Por fim, outra grandeza é a raiz da velocidade quadrática média, que fornece a velocidade de uma partícula que possui o valor médio de energia cinética dentre as partículas do gás.
Uma curiosidade dessa última forma de medir é sua relação íntima com a velocidade do som num gás. Abaixo, $f$ representa os graus de liberdade de uma única partícula — quantidade de maneiras que ela pode se movimentar, incluindo translação, rotação e vibração.
Quando voltamos os olhares para a energia cinética das partículas de um gás, é possível calcular a partir da expressão $E_C = \dfrac{3}{2}pV=\dfrac{3}{2}nRT$, para uma soma da energia cinética de todas as partículas, ou $E_C=\dfrac{3}{2}k_BT$, para a energia cinética média associada a uma única partícula.
Transformações gasosas
Chamamos transformação gasosa todo processo físico caracterizado pela mudança do estado inicial de um gás, ou seja, em seu volume, pressão ou temperatura. Em sistemas fechados (sem alteração do número de partículas do gás), são identificáveis três tipos de transformações: isobáricas, isovolumétricas e isotérmicas.
A importância do estudo das transformações gasosas está na sua aplicação, central para a termodinâmica, mencionada no início do documento — pelas transformações gasosas é possível extrair trabalho do gás.
Nas transformações chamadas isobáricas (do grego para “peso”, que originou o prefixo para pressão), temos a conservação da pressão do começo ao fim do processo. A conservação da pressão implica na mudança do volume e da temperatura do gás.
Considerando o índice 1 como o estado inicial e o índice 2 como após o processo, é possível ver o estabelecimento de uma relação linear entre o volume e a temperatura de um gás.
Nas transformações chamadas isovolumétricas ou isocóricas (do grego “khorus”, “espaço”), o volume do gás permanece constante ao longo do tempo, enquanto sua pressão e sua temperatura sofrem variação. De forma similar, é estabelecida uma relação linear entre a pressão e a temperatura.
Finalmente, nas transformações conhecidas por isotérmicas, temos a conservação da temperatura do gás ao longo do tempo e a variação de seu volume e de sua pressão. Diferentemente das outras duas transformações, é estabelecida uma relação hiperbólica entre as grandezas variáveis.
Energia interna
Definimos a energia interna de um gás como a energia total do gás, a soma da energia cinética de suas partículas (além das interações intra e intermoleculares), quando seu centro de massa está em repouso. Seguindo nosso padrão de aproximação, calculamos a energia interna pela expressão abaixo.
Uma característica notável é a possibilidade de classificar as transformações gasosas, vistas acima, a partir da mudança de energia interna do gás. Pela dependência da energia interna na temperatura, podemos ver que enquanto ela permanece constante em transformações isotérmicas, o mesmo não acontece nas restantes.
Trabalho termodinâmico
O trabalho termodinâmico, também conhecido pela denominação trabalho volume-pressão, é o trabalho exercido pela compressão ou expansão de fluidos, e acontece sempre em transformações isobáricas.
Durante a execução desse trabalho por máquinas, tanto a compressão quanto a expansão do fluido pode ocorrer. Nos momentos de compressão, o gás ganha energia (com trabalho sendo realizado sobre ele); nos momentos de expansão, o gás cede energia realizando trabalho.
A expressão matemática para encontrar o trabalho realizado pode ser deduzida por meio de uma análise relativamente simples, apoiada pela figura ao lado.
Partindo de que a expressão para o trabalho de uma força paralela ao deslocamento do corpo é $\tau = Fd$, é possível reescrever a equação de diferentes maneiras.
Dessa forma, percebemos que o trabalho realizado (ou sofrido) pelo gás está diretamente relacionado com a variação de seu volume, em pressões constantes.
Em casos mais gerais, em que essa expressão pode não se aplicar, o trabalho é dado como a “área sob a curva” de um gráfico pressão vs volume, a integral.
.*](./images/introduction_thermodynamics/introduction_thermodynamics_pvwork.png)
Figura ilustrando o processo do trabalho volume-pressão. Imagem licensiada sob CC-BY, via OpenStax Physics.
Ciclos Termodinâmicos — Carnot, Otto e Diesel
Chamamos ciclos termodinâmicos as sequências de processos termodinâmicos exercidos num sistema que, após um certo número de processos, retornam o sistema ao estado original. Ciclos termodinâmicos são comuns em motores, com alguns destacando-se pela sua utilização na indústria moderna ou no estudo científico. São eles os ciclos de Carnot, Otto e Diesel.
Ciclo de Carnot
O ciclo de Carnot, nomeado em homenagem ao seu idealizador, o físico francês Sadi Carnot (1796 — 1832), é um ciclo termodinâmico ideal executado pela máquina de Carnot, a mais eficiente máquina térmica possível fisicamente, mas impossível de ser plenamente construída: o físico idealizou sua máquina como um padrão ideal para mensurar a eficiência de máquinas térmicas reais.
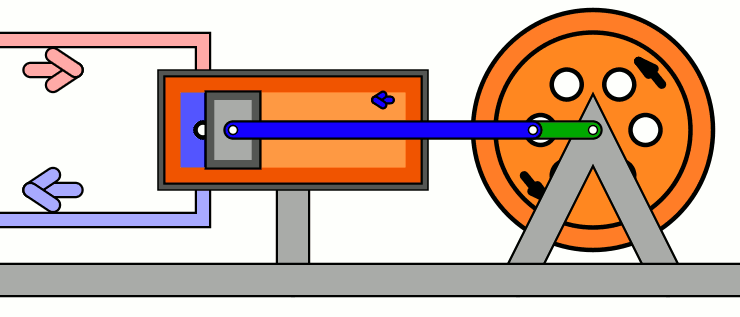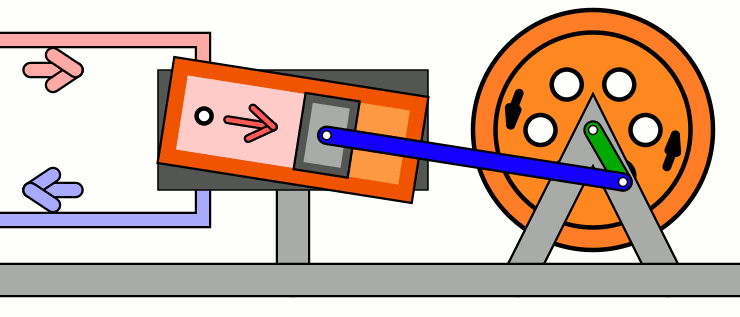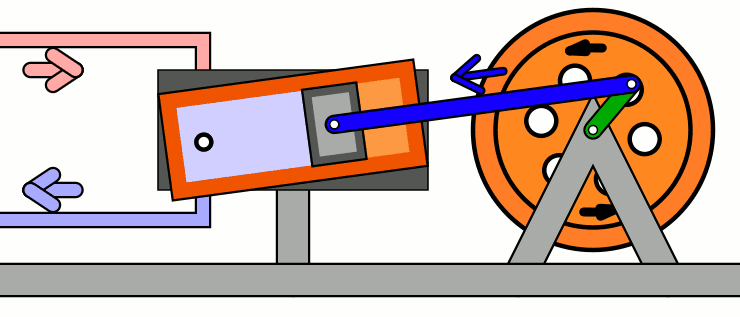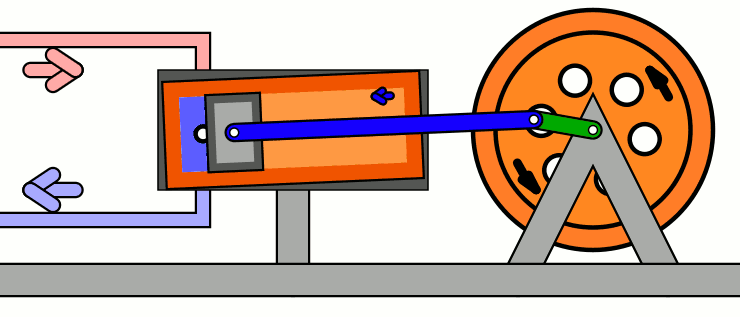
Carnot, ao desenhar seu ciclo, tinha em mente primariamente as máquinas térmicas dominantes de seu tempo — motores à vapor. GIF por MichaelFrey via Wikimedia Commons (CC-BY-SA)
A máquina ideal de Carnot é dividida entre uma fonte (ou “reservatório”) quente, que fornece energia térmica ao gás (uma lareira, um aquecedor elétrico, …) e uma fonte (ou “reservatório”) fria, que absorve a energia térmica do gás. O gás está situado entre essas duas fontes e pode ser exposto ou isolado delas por barreiras adiabáticas. Sobre o gás está situado um pistão, que terá trabalho exercido sobre ele.
O ciclo é dividido em quatro etapas — duas expansões e duas compressões — isotérmicas e adiabáticas.
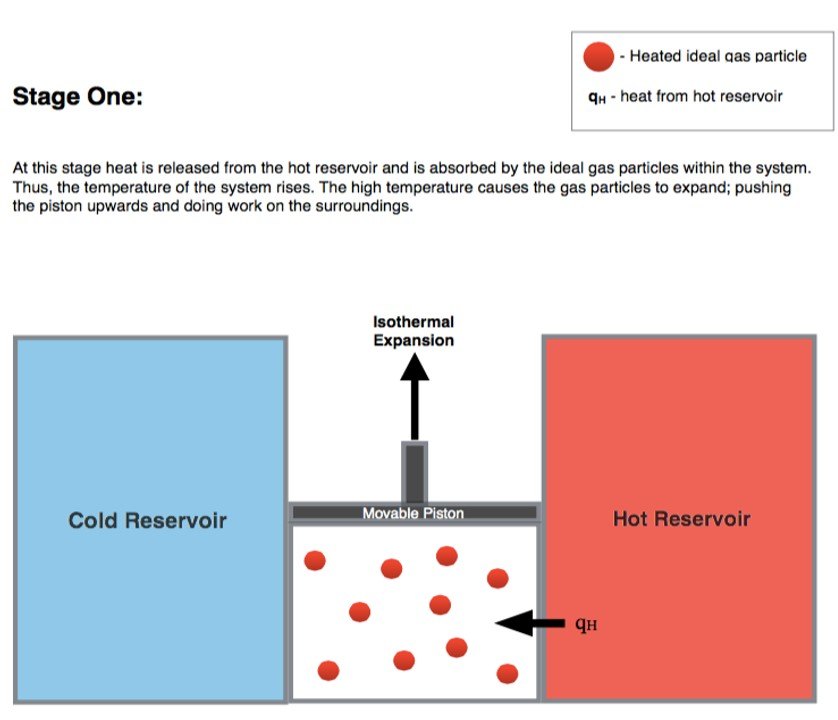
Por “Blyumj”, via Wikimedia Commons (CC-BY-SA)
- Expansão isotérmica: o gás sofre uma expansão isotérmica ao ser exposto à fonte quente. Nesse passo, o gás possui uma temperatura infinitesimalmente menor que essa fonte, permitindo uma absorção de calor com uma mudança negligível da temperatura do gás;
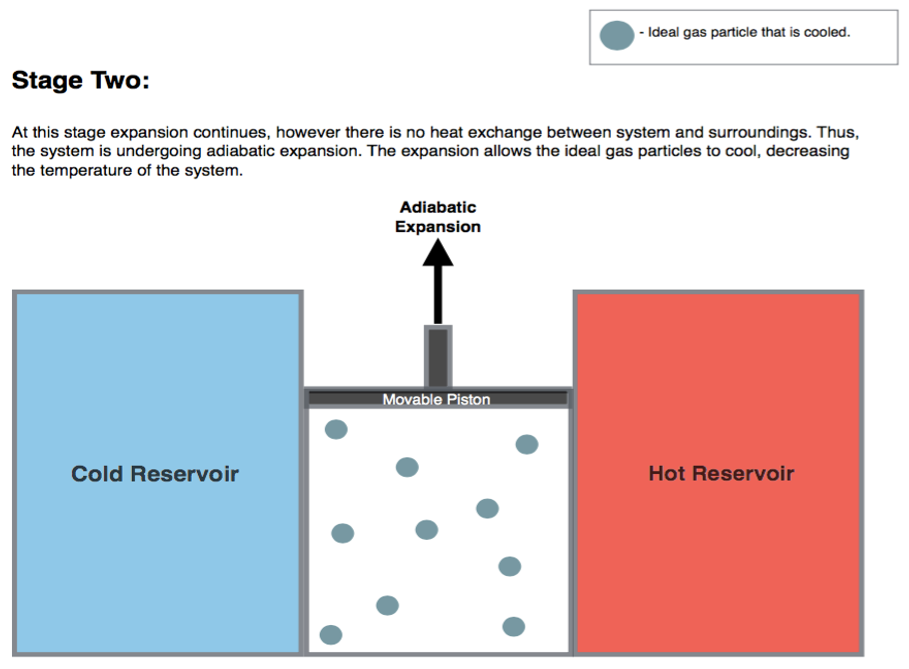
Por “Blyumj”, via Wikimedia Commons (CC-BY-SA)
- Expansão adiabática: o gás é isolado da fonte quente e continua a se expandir num processo adiabático, exercendo trabalho no pistão. Esse trabalho causa o resfriamento do gás, que neste passo é resfriado até atingir uma temperatura infinitesimalmente maior que a temperatura da fonte fria;
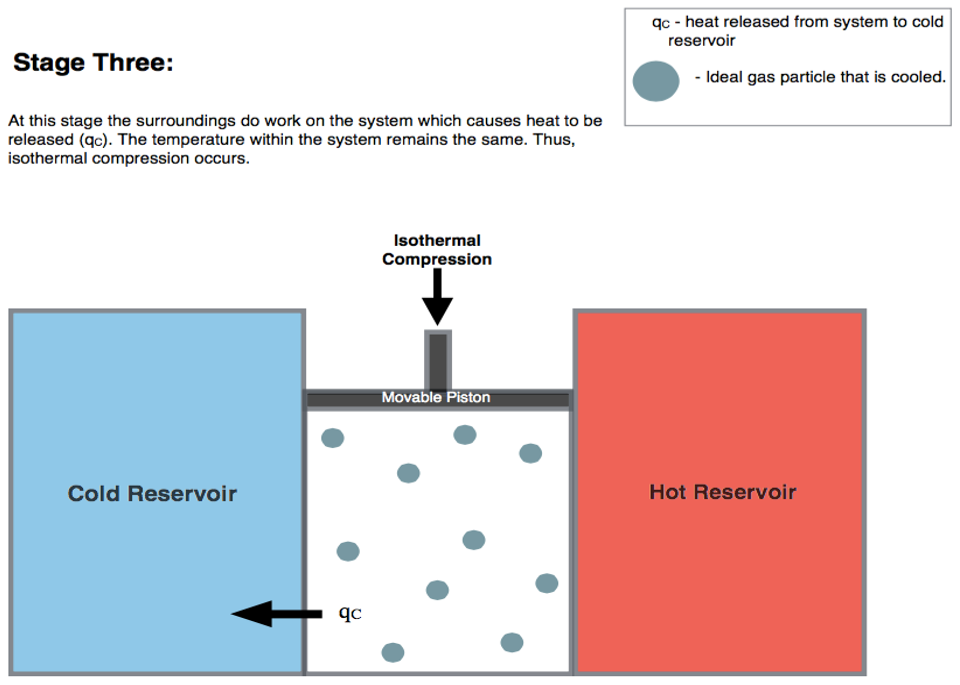
Por “Blyumj”, via Wikimedia Commons (CC-BY-SA)
- Compressão isotérmica: o gás cede calor para a fonte fria, estando isolado termicamente da fonte quente. Perdendo energia, sofre uma compressão isotérmica de forma semelhante ao passo 1.
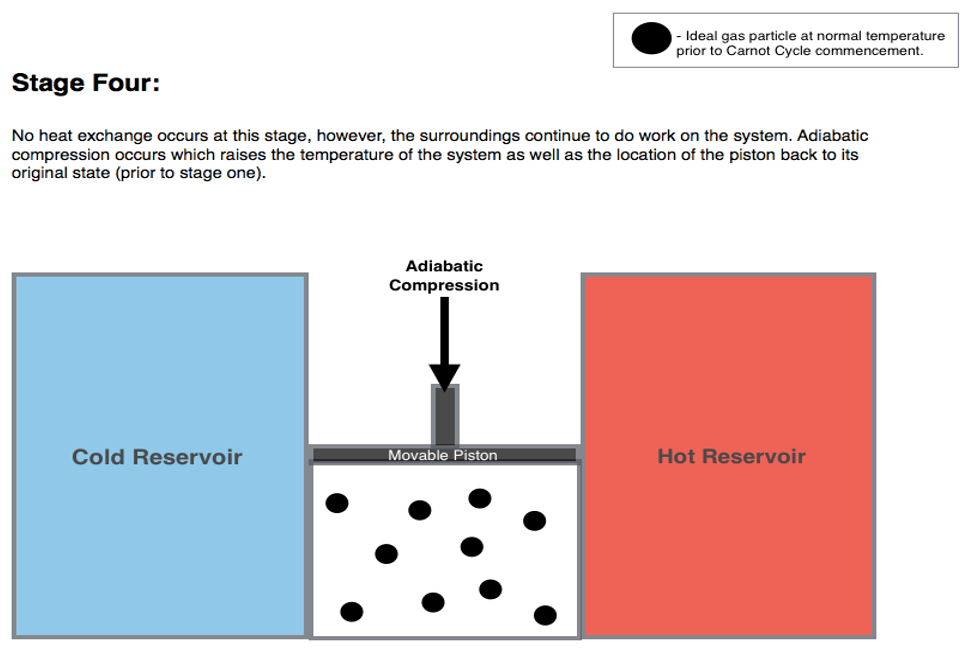
Por “Blyumj”, via Wikimedia Commons (CC-BY-SA)
- Compressão adiabática: o gás é isolado termicamente das duas fontes, com o exterior continuando a realizar trabalho sobre o gás, comprimindo-o num processo adiabático. Sua energia interna aumenta até os níveis iniciais, retornando o sistema para o estado inicial e concluindo o ciclo.
Neste ciclo o trabalho exercido pelo gás está nas etapas de expansão, com os limites da eficiência do motor estando nas temperaturas das fontes. De fato, podemos mensurar a eficiência da máquina de Carnot pela expressão a seguir.
Ciclo de Otto
O ciclo de Otto também é um ciclo termodinâmico ideal, porém com um propósito diferente.
Nomeado em homenagem ao engenheiro alemão Nicolaus Otto (1832 — 1891), o ciclo descreve o funcionamento ideal de um motor de combustão interna de ignição à vela, como os encontrados em automóveis.
Embora ele também possa ser descrito para motores “de dois tempos”, o ciclo abaixo descrito será o de quatro tempos.

Nicolaus Otto, c. 1868. O engenheiro fundou a Deutz, que fabrica motores até hoje. Seu filho, Gustav Otto, fundou uma das empresas precursoras da BMW.
- Compressão adiabática: a mistura ar-combustível é comprimida pelo pistão, aumentando sua temperatura, num processo adiabático;
- Ignição: o combustível é denotado pela vela do motor, gerando uma mistura gasosa altamente pressurizada e com alta energia inteira. Essa etapa pode ser descrita como um processo isocórico;
- Expansão adiabática: o gás exerce trabalho sobre o pistão do motor ao expandir-se sem trocar calor com o ambiente;
- Expulsão do calor e do combustível residual: a energia térmica residual do processo, além do restante da mistura ar-combustível não detonada, é expulsa, com novo ar entrando no motor. O motor está de volta ao estado inicial pronto para voltar ao passo 1.
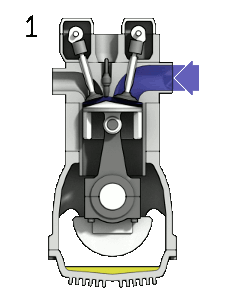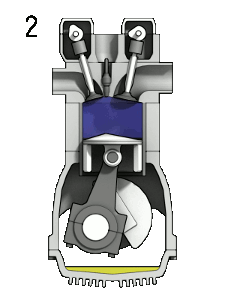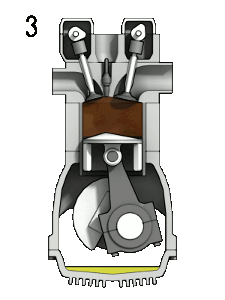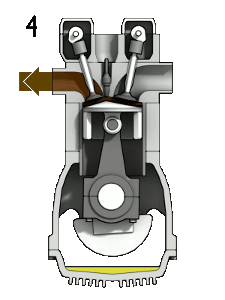
Animação demonstrando o funcionamento do motor de quatro tempos. Por Zephyris, via Wikimedia Commons (CC-BY-SA)
Ciclo de Diesel
O ciclo de Diesel, nomeado em homenagem ao inventor franco-alemão Rudolf Diesel (1858 — 1913), é bem similar ao ciclo de Otto, porém com uma diferença chave: a ausência do detonador presente nos motores à gasolina. Os motores Diesel são arquitetados com a autodetonação do combustível em mente, sendo mais eficientes, embora mais difíceis de construir e manter.
Este ciclo termodinâmico pode ser descrito de forma didática em seis passos.
- Entrada de ar no motor;
- Compressão adiabática do ar pelo pistão;
- Injeção de combustível, que se mistura com o ar comprimido, detonando-se e empurrando o pistão numa expansão isobárica;
- Com o fim da combustão de todo o combustível, o gás quente continua expandindo-se abiabaticamente;
- Válvula de escape aberta, queda abrupta da pressão no interior do cilindro, que equaliza-se com a pressão atmosférica;
- Expulsão de resíduos e do gás do interior do cilindro;
.](./images/introduction_thermodynamics/introduction_thermodynamics_fourstroke.png)
Funcionamento de um motor Diesel. Imagem original daqui.