Introdução à Química Orgânica
Uma breve origem da Química Orgânica
No século XVIII, em 1777, Bergman, químico sueco, dividiu a crescente ciência da Química em duas áreas, a química inorgânica, química dos “minerais”, e a química orgânica, a “química dos seres vivos”.
Nesse mesmo período, havia a teoria da força vital, notavelmente defendida pelo químico sueco Berzelius em 1807, que dizia que somente os seres vivos podiam produzir, sintetizar, produtos orgânicos, produtos esses que Lavoisier verificou a presença de carbono em todos eles.
Porém, em 1828, essa teoria, muito influente, foi derrubada pelo químico alemão Friedrich Wöhler: ele conseguiu sintetizar ureia (presente na urina) a partir de compostos inorgânicos, o que a teoria da Força Vital via como impossível.
Trinta anos depois, Friedrich August Kekulé, químico alemão, em meio a toda enfervescência científica do período, propôs à Academia uma nova maneira de definir a química orgânica, maneira essa que acabou sendo utilizada até hoje — a Química orgânica é a seção da química preocupada de forma especial com o Carbono e suas interações.
Postulados de Kekulé
Além disso, Kekulé propôs alguns postulados, bases, para todo o estudo da química orgânica, referentes ao seu elemento central, o Carbono.
Hibridação
O motivo do carbono conseguir sempre formar quatro ligações é o fenômeno da hibridação.
A hibridação (ou hibridização) de orbitais acontece quando elétrons de orbitais completos saltam para outro orbital em outro subnível ao receberem energia, permitindo mais ligações e efetivamente “combinando” os subníveis numa única estrutura: orbitais híbridos foram formados.
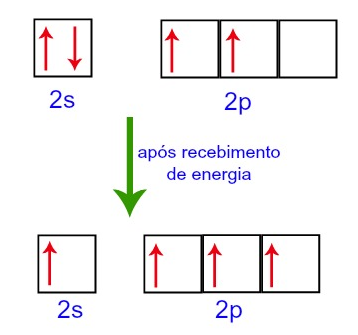
No começo, o carbono só poderia formar duas ligações…
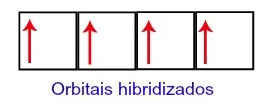
…mas com o salto e a combinação dos orbitais, agora ele consegue formar quatro!
Existem vários tipos de hibridação, com cada uma delas representando quais orbitais foram hibridizados. Cada uma delas também possui um efeito diferente na geometria da molécula, por conta da repulsão dos elétrons livres.
| Tipo | Orbitais hibridizados | Geometria | Exemplo |
|---|---|---|---|
| sp | 1s + 1p | Linear (180º) | BeCl2, acetileno |
| sp² | 1s + 2p | Trigonal plana (120º) | BF3, etileno |
| sp³ | 1s + 3p | Tetraédrica (109.5°) | CH4 |
| sp³d | 1s + 3p + 1d | Trigonal bipiramidal | PCl5 |
| sp³d² | 1s + 3d + 2d | Octaédrica | SF6 |
Entretanto, como o carbono é tetravalente sempre, podemos restringir a tabela para apenas três casos:
| Número de ligações | Tipo da hibridação | Geometria |
|---|---|---|
| 4 | sp³ | Tetraédrica (109.5°) |
| 3 | sp² | Trigonal plana (120°) |
| 2 | sp | Linear (180°) |
Um exemplo da primeira linha é a molécula de metano $(\text{CH}_4)$, o hidrocarboneto mais simples e comumente encontrado em depósitos de petróleo.
O carbono central da ligação possui quatro ligações: todas são simples em razão de sua tetravalência.
Um exemplo para a segunda linha é o formaldeído $(\text{CH}_2\text{O})$ ou metanal, conhecido mais comumente em sua forma diluída, o formol, utilizado para conservação de cadáveres, por exemplo.
O primeiro exemplo para a terceira linha pode ser dado pelo cianeto de hidrogênio $(\text{HCN})$, um composto extremamente volátil, inflamável e tóxico. Seu uso mais famoso foi durante a Segunda Guerra Mundial pela Alemanha Nazista nos campos de extermínio, onde era conhecido pelo seu nome comercial: Zyklon B.
Por fim, o segundo exemplo para a terceira linha é o dióxido de carbono $(\text{CO}_2)$, gás produzido pela humanidade em grande volume desde o início da Revolução Industrial. É um dos grandes responsáveis pela intensificação do efeito estufa.